
Đang tải...

Đang tải...
Tác giả: Lakshmanan D1 , Sashank Pillai1, Rahul Baghla2 and Eshani Galermo2
1 SCIEX, India and 2SCIEX, USA
Tóm tắt kỹ thuật
Ghi chú kỹ thuật này trình bày một phương pháp nhạy để định lượng pasireotide trong huyết tương người bằng cách sử dụng kỹ thuật khối phổ phân giải cao, độ chính xác khối cao (Tứ cực thời gian bay kết hợp với bẫy ion tuyến tính Zeno). Giới hạn định lượng dưới (LLOQ) đạt mức 0,05 ng/mL trong các mẫu huyết tương sau chiết xuất (Hình 1). MRMHR là kỹ thuật ghi MRM trên các hệ thống QTOF của SCIEX như SCIEX X500R/B, ZenoTOF 7600/7600+/8600, trong đó ion mẹ được phân lập sử dụng tứ cực tương tự như cách vận hành của các hệ ba tứ cực (QqQ), nhưng thay vì chỉ theo dõi lần lượt 1-2 ion phân mảnh, MRMHR quét và ghi đồng thời phổ tất cả các ion phân mảnh (Full scan MS2), sau đó SCIEX OS sẽ tự động lựa chọn ion phân mảnh phù hợp nhất để tiến hành định lượng. Kết hợp với bẫy Zeno, quy trình định lượng chất phân tích với MRMHR cho độ nhạy và độ chọn lọc vượt trội so với chỉ sử dụng MS1 kể cả ở chế độ phân giải cao.
Pasireotide là một loại thuốc hexapeptide vòng được đưa vào sử dụng từ năm 2012 để điều trị bệnh Cushing. Pasireotide là thuốc tác động lên tuyến yên, giúp giảm bài tiết cortisol từ tuyến thượng thận. Do vai trò then chốt trong điều trị bệnh Cushing, việc tạo điều kiện thuận lợi để đo lường hiệu quả pasireotide ở các mức nồng độ độc động học và dược động học trong các nền mẫu sinh học là rất thiết yếu.
Ghi chú kỹ thuật này chứng minh một quy trình làm việc đáng tin cậy và có độ nhạy cao nhằm hỗ trợ phân tích định lượng pasireotide trong huyết tương người bằng máy khối phổ phân giải cao, khối lượng chính xác.

Hình 1: Sắc ký đồ ion chiết (XIC) đại diện của mẫu trắng nền (matrix blank), mức 0,05 ng/mL (LLOQ) và 0,1 ng/mL (mẫu kiểm soát chất lượng mức thấp, LQC) đối với pasireotide trong huyết tương người sau chiết xuất.
I Giới thiệu
Vào năm 2012, Pasireotide đã được phê duyệt để điều trị cho bệnh nhân trưởng thành mắc bệnh Cushing tại cả EU và Hoa Kỳ. Thuốc được chỉ định cụ thể cho những người không đủ điều kiện phẫu thuật hoặc không thấy cải thiện sau điều trị. Pasireotide được giới thiệu như một giải pháp thay thế cho somatostatin (lựa chọn điều trị trước đó vốn gặp thách thức do chu kỳ bán rã ngắn). Cấu trúc của pasireotide bao gồm một cầu nối disulfide, giúp tăng cường độ ổn định chuyển hóa và làm cho nó phù hợp để duy trì hiệu quả dược lý kéo dài.
Do đó, cấu trúc phức tạp của các liệu pháp peptide vòng như pasireotide đòi hỏi các phép thử có độ chọn lọc và độ nhạy cao để đảm bảo phát hiện và định lượng chính xác khi đánh giá các tác động dược động học và dược lực học.
II Phương pháp
Chuẩn bị chất chuẩn: Dung dịch chuẩn gốc pasireotide (1 mg) được mua từ Medchem Express và hòa tan trong dung dịch axit formic 0,1% pha trong hỗn hợp acetonitrile/nước tỉ lệ 50:50 (v/v). Các lần pha loãng tiếp theo được thực hiện trong axit formic 0,1% pha trong hỗn hợp acetonitrile/nước tỉ lệ 20:80 (v/v).
Chuẩn bị mẫu: Pasireotide (từ 0,05 đến 1000 ng/mL) được thêm vào 100 µL huyết tương. Một thể tích tương đương đệm TRIS 50mM được thêm vào huyết tương và vortex. Các mẫu được thực hiện chiết pha rắn (SPE) bằng đĩa 96 giếng Phenomenex Strata-X Polymeric Reverse Phase, 2mg. Sau khi nạp mẫu, mẫu được rửa bằng nước chứa 1% axit acetic trong hỗn hợp nước/methanol tỉ lệ 95:5 (v/v). Quá trình giải hấp (elution) được thực hiện với 200 µL methanol và làm khô bằng dòng khí nitơ nhẹ. Các mẫu sau đó được hoàn nguyên với 100 µL hỗn hợp acetonitrile chứa 0,1% axit formic/nước chứa 0,1% axit formic tỉ lệ 20:80 (v/v).
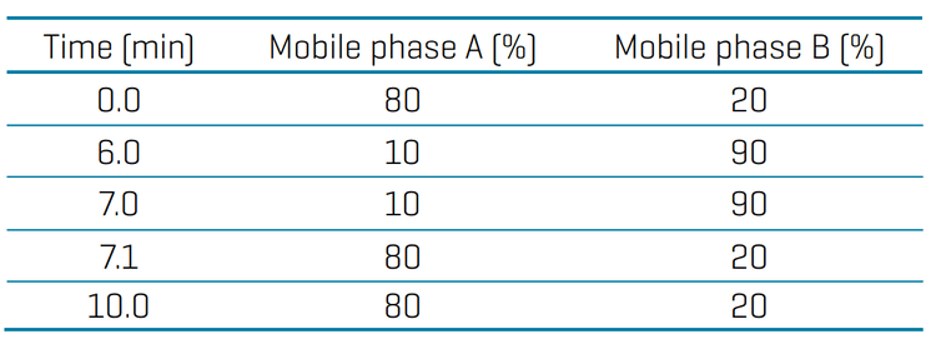
Sắc ký: Việc tách phân tích được thực hiện trên hệ thống ExionLC AE sử dụng cột Phenomenex Kinetex C18 (2,1 × 100 mm, 1,7 µm) ở tốc độ dòng 0,3 mL/phút. Pha động A là axit formic 0,1% trong nước và pha động B là axit formic 0,1% trong acetonitrile. Nhiệt độ cột được đặt ở 55°C. Các điều kiện gradient được tóm tắt trong Bảng 1. Một lượng mẫu 20 µL được tiêm để phân tích LC-MS/MS.
Bảng 1: Các điều kiện gradient LC cho pasireotide.
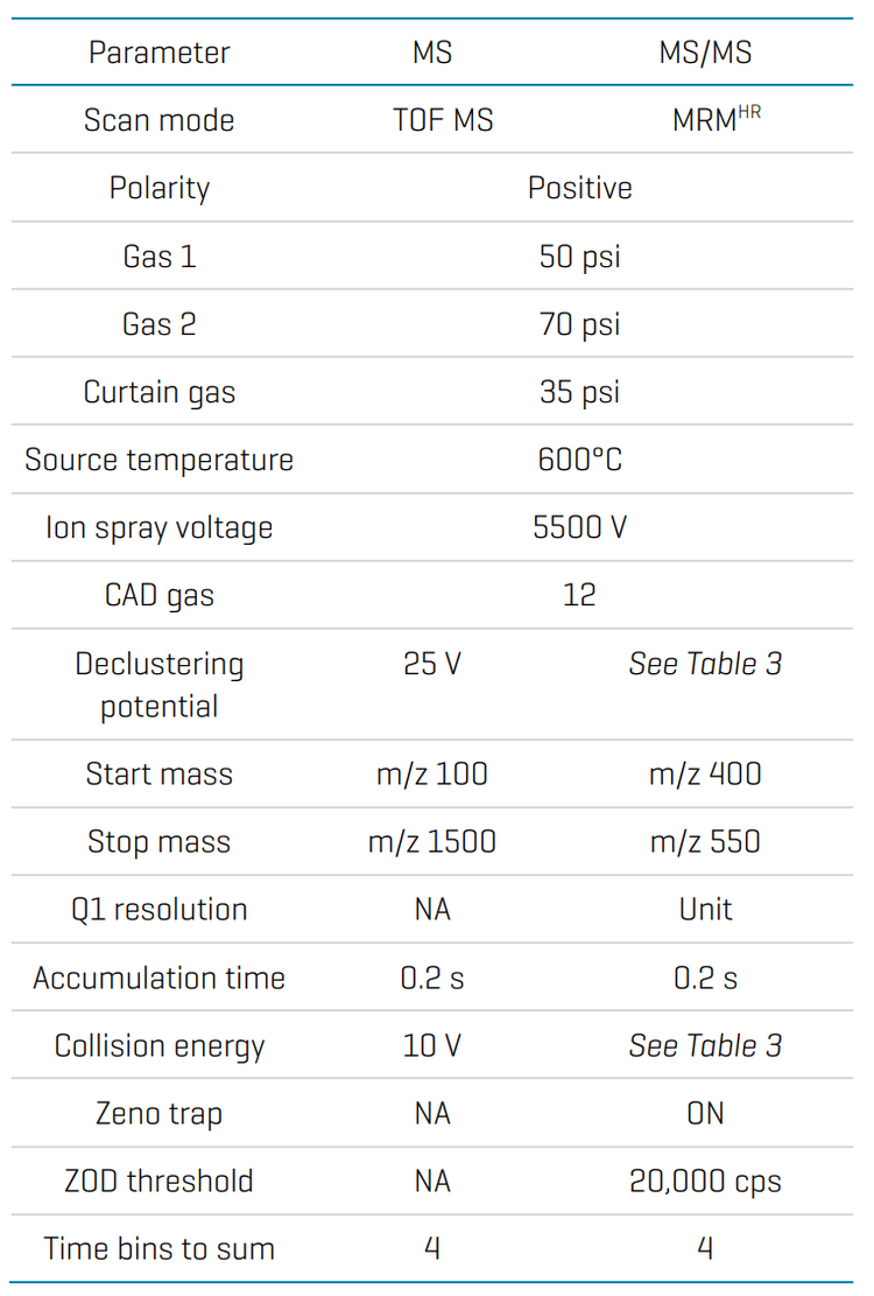
Khối phổ: Các mẫu được phân tích bằng hệ thống ZenoTOF 7600 vận hành ở chế độ ion dương. Dữ liệu được thu nhận bằng thí nghiệm Zeno MRMHR. Các thông số MS tối ưu hóa được liệt kê trong Bảng 2. Tóm tắt các thông số Zeno MRMHR được hiển thị trong Bảng 3.
Bảng 2: Các điều kiện nguồn, khí và hệ thống ZenoTOF 7600.
Bảng 3: Các thông số Zeno MRMHR được sử dụng để định lượng.

Xử lý dữ liệu: Phân tích được thực hiện bằng phần mềm SCIEX OS, phiên bản 3.3.1. Các pic được tích phân bằng thuật toán MQ4 và sử dụng trọng số 1/x² để định lượng pasireotide. Độ rộng pic XIC là 0,05 Da được áp dụng để định lượng.
III Hiệu suất định lượng trên hệ thống ZenoTOF 7600
Các liệu pháp peptide vòng như pasireotide chứa cầu nối disulfide, thường gây ra những thách thức trong quá trình phân mảnh. Bước đánh giá ban đầu được thực hiện với chế độ Zeno MS1 (đo từ ion mẹ sang ion mẹ mà không phân mảnh). Cách tiếp cận này được so sánh với Zeno MRMHR (áp dụng CID và đo ion con). Sắc ký đồ mẫu trắng nền được đánh giá giữa hai chế độ Zeno MS1 và Zeno MRMHR. So với Zeno MRMHR, chế độ Zeno MS1 cho thấy độ chọn lọc thấp hơn với nền nhiễu cao hơn trong các mẫu huyết tương sau chiết xuất (Hình 2).
Kết quả là, phương pháp Zeno MRMHR đã được sử dụng để đạt được độ chọn lọc và độ nhạy tốt hơn nhằm định lượng pasireotide trong huyết tương người. Hiệu suất cải thiện trong việc lấy mẫu MS/MS tổng số với bẫy Zeno (Zeno trap) trên hệ thống ZenoTOF 7600 khiến nó trở thành một công cụ giá trị cho các quy trình định lượng đòi hỏi độ nhạy và độ chọn lọc cao.
Sử dụng Zeno MRMHR, một đường chuẩn đã được phân tích cho pasireotide ở các nồng độ từ 0,05 đến 1000 ng/mL. Để đánh giá độ lặp lại, mỗi nồng độ chuẩn được phân tích lặp lại 3 lần. LLOQ đạt mức 0,05 ng/mL với thể tích huyết tương tối thiểu là 100 µL (Hình 1). Không quan sát thấy nhiễu nền tại thời gian lưu của chất phân tích.
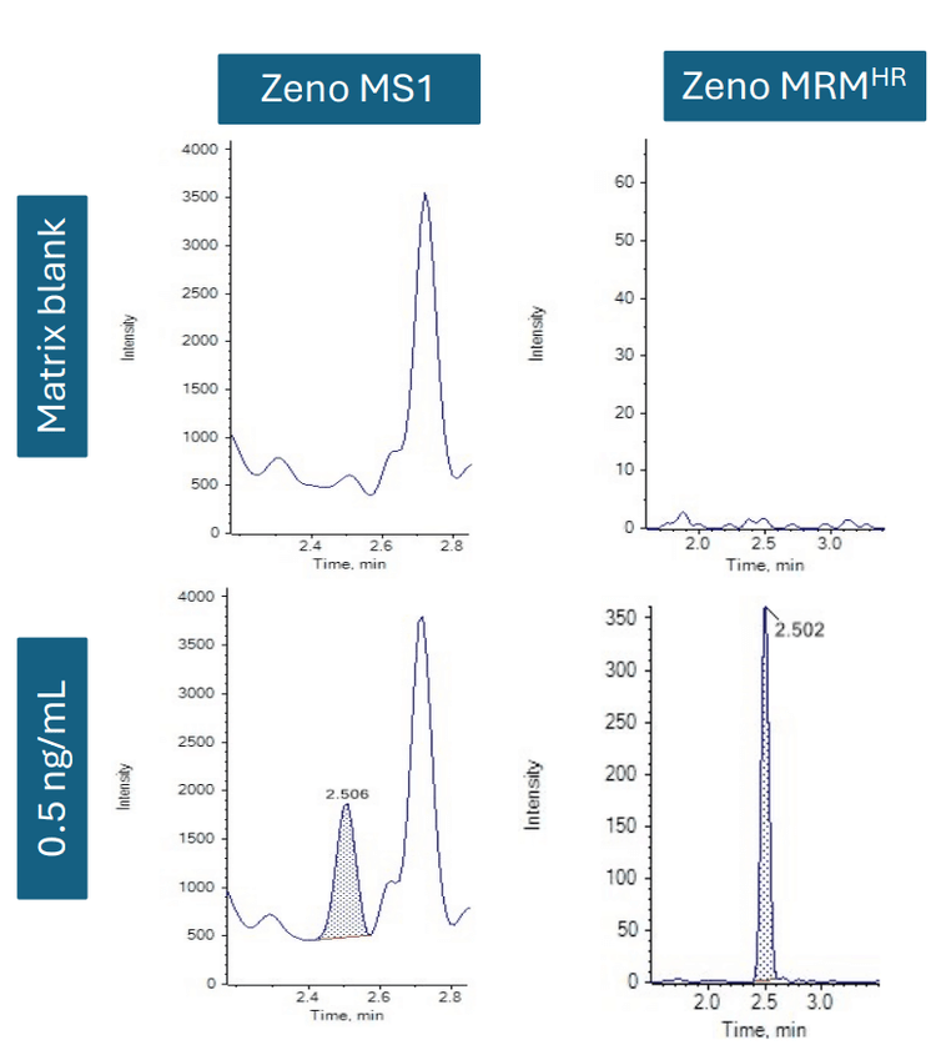
Hình 2: XIC đại diện của mẫu trắng nền (trên) và mức 0,5 ng/mL (dưới) của pasireotide trong huyết tương người sử dụng Zeno MS1 (trái) và Zeno MRMHR (phải). Nền nhiễu cao hơn được quan sát thấy tại thời gian lưu của chất phân tích khi sử dụng Zeno MS1 so với Zeno MRMHR.
Độ tuyến tính đạt được trên các nồng độ từ 0,05 đến 1000 ng/mL với hệ số xác định (r²) >0,994 (Hình 3), đạt được khoảng động tuyến tính (LDR) là 4,3 bậc độ lớn.
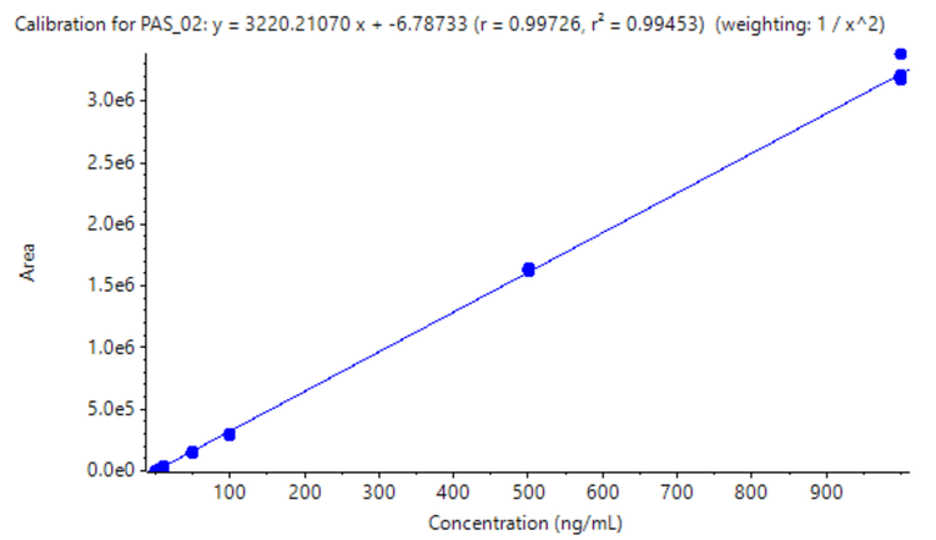
Hình 3: Đường chuẩn định lượng pasireotide với hệ số trọng số 1/x².
Hiệu suất phân tích được đánh giá dựa trên yêu cầu: độ chính xác của giá trị trung bình tính toán phải nằm trong khoảng 80% đến 120% tại mức LLOQ và từ 85% đến 115% tại các nồng độ cao hơn. Hệ số biến thiên (%CV) của giá trị trung bình nồng độ phải dưới 20% tại LLOQ và dưới 15% tại tất cả các nồng độ cao hơn. Đối với phép thử này, độ chính xác nằm trong khoảng ±16% so với nồng độ danh định và %CV <11% đối với pasireotide trong huyết tương người (Hình 4). Các giá trị độ chính xác và %CV tính toán đều nằm trong tiêu chí chấp nhận tại mỗi mức nồng độ.
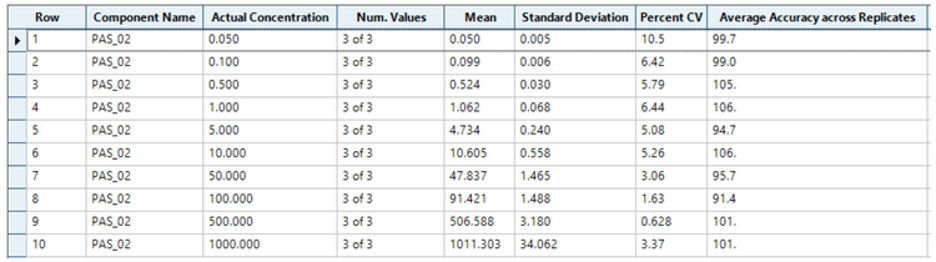
Hình 4: Hiệu suất định lượng cho phân tích pasireotide (m/z 524,3 → m/z 427,231). Kết quả độ lặp lại và độ chính xác được xác định từ các điểm đường chuẩn qua 3 lần lặp tại mỗi nồng độ. Kết quả thống kê được tóm tắt bằng mô-đun Analytics trong phần mềm SCIEX OS.
IV Phần mềm SCIEX OS sẵn sàng cho các tiêu chuẩncần tuân thủ
Các khả năng tương đương của phần mềm SCIEX OS cho phân tích sinh học có kiểm soát (regulated bioanalysis) có thể được thực hiện trên hệ thống SCIEX 7600, đảm bảo độ tin cậy cao khi chuyển đổi phương pháp trong khi vẫn duy trì các tính năng tuân thủ quan trọng.
Phần mềm SCIEX OS là một hệ thống kín và yêu cầu các hồ sơ cũng như chữ ký phải được lưu trữ điện tử, đáp ứng các quy định được nêu trong tiêu chuẩn 21 CFR Phần 11. SCIEX OS có thể mở các tệp dữ liệu thô từ bất kỳ vị trí lưu trữ hiển thị nào trong mạng nội bộ bằng cách sử dụng các trạm làm việc xử lý chuyên dụng. Hình 5 minh họa các tính năng của phần mềm SCIEX OS được sử dụng để giám sát nhật ký hệ thống (audit trail), thu nhận và xử lý dữ liệu, cũng như cấu hình quyền truy cập của người dùng. Tính năng nhật ký hệ thống cho phép người dùng kiểm tra các hành động quan trọng của người dùng và khóa tính toàn vẹn của dữ liệu. Tính năng Bảng điều khiển Quản trị Trung tâm (CAC) cho phép người dùng tập trung hóa việc thu nhận và xử lý bằng một nền tảng duy nhất để tối đa hóa hiệu quả cho các phòng thí nghiệm đa thiết bị, độc lập với các tiêu chuẩn tuân thủ. Mô-đun cấu hình cho phép người dùng chỉ định các vai trò và quyền truy cập như quản trị viên, người phát triển phương pháp, phân tích viên và người phê duyệt.

Hình 5: Các tính năng của phần mềm SCIEX OS để giám sát quyền truy cập của người dùng và đánh giá nhật ký hệ thống. Chế độ xem nhật ký hệ thống cho phép người dùng dễ dàng lọc các sự kiện có rủi ro cao và kích hoạt các tính năng toàn vẹn dữ liệu để đáp ứng các yêu cầu tuân thủ. Phần mềm có Bảng điều khiển Quản trị Trung tâm (CAC) để quản lý người dùng và nhóm, định nghĩa vai trò, trạm làm việc và dự án trên tất cả các hệ thống. Tính năng CAC hỗ trợ cả các tiêu chuẩn tuân thủ có kiểm soát và không kiểm soát. Mô-đun cấu hình cho phép người dùng nhanh chóng thiết lập các vai trò và mức độ truy cập cho các cấp độ quản trị viên, người phát triển phương pháp, phân tích viên và người phê duyệt.
V Kết luận